摘要
四面体碳立体中心的控制仍然是现代合成化学的一个焦点,并使其构型的稳定性。相比之下,三取代氮1、磷2硫化合物3.经历金字塔反转,一个基本的和公认的立体化学现象,被广泛利用4.然而,氧鎓离子(一个带正电的氧原子上有三个取代基的化合物)的立体化学还不太发达,除了作为反应中间体之外,氧鎓离子在合成中的应用很少5,6.在构型稳定的氧离子中,没有氧原子是唯一立体中心的例子,可能是由于氧金字塔反转的低势垒7所有氧鎓离子都是高活性的。在这里,我们描述了一种螺旋手性三芳氧氧鎓离子的设计、合成和表征,其中氧孤对的反转通过几何限制被阻止,使其能够作为构型的决定因素。合成和量子计算相结合的方法描述了能够生成配置稳定和室温可分离盐的设计原则。我们发现反转势垒大于110 kJ mol−1并概述解决方案的流程。据我们所知,这是唯一一个以氧原子为唯一立体中心的手性非外消旋和构型稳定的分子。
主要
三取代胺、膦和磺胺盐的锥体转化是一种基本的立体化学过程,已经得到了深入的研究,从而了解了影响其转化障碍大小的因素1.这使得生成无数构型稳定的手性膦(具有120 - 185kj mol的反转势垒)成为可能−1)3.和硫盐(屏障100-130 kJ mol)−1)4.叔胺中氮原子的转化具有较低的势垒(20-25 kJ mol)−1),量子隧穿效应对观测到的速率有很大贡献2;这意味着制备具有立体氮原子的构型稳定的叔胺是特别具有挑战性的。然而,有许多双环胺的例子,如Tröger的碱18,9,10金鸡纳生物碱11和其他人12,13其中,由于构象刚性,氮的倒置受到限制,从而可以获得含有立体氮的化合物(图2)。1)14.相比之下,对氧离子的研究要落后得多15,16.三价氧化合物反转势垒的唯一经验测量是对环氧化物衍生的氧鎓盐2可逆势垒为42kj mol−1,这大大低于在环境温度下保持构型稳定性所需的温度7.因此,没有分离出富氧对映体氧离子的例子,其中氧原子17,18是唯一的立体中心(图2)。1 b)。
氧离子被认为是高活性的,在包括天然产物生物合成和全合成在内的一系列合成转化中被用作瞬态中间体19,20.,21,22,23,24.这导致了复杂的三烷基氧鎓离子的表征,如3.一种被提议用于合成Laurencia家族天然产物的中间体。熔断环系统3.防止反转,因此氧是立体的;在这种情况下,氧离子以非对映选择性的方式由带有几个碳立体中心的前驱体形成5.四环氧鎓离子4由于其不对称的桥,具有一个立体氧25.最有名的氧鎓离子可以说是四氟硼酸三烷基,它在80多年前由Meerwein首次合成6,26.虽然它们稳定且可分离,但它们也是合成化学实验室中使用的一些最活跃的烷基化剂,并且很容易与弱亲核试剂(包括水)反应。其它的烷基氧鎓离子也被制备和研究过27,28,29,30.但对亲核试剂稳定的物种是难以捉摸的,直到Mascal报道了oxatriquinane oxonium离子31,32,33,34;这表明在环结构中嵌入氧离子对稳定性的潜在影响。与大多数烷基取代氧鎓离子相比,简单的三芳氧鎓离子几乎是围绕氧的三角平面,是稳定的可分离固体,抵抗许多亲核试剂的作用35,36,37.二苯并呋喃衍生的三芳氧鎓离子在氧原子上呈锥体状38这促使鲍德里奇和西格尔研究氧鎓盐中外环C-O键的旋转5(右1= Et, R2= H);这表明势垒(估计大于84 kJ mol)−1)可能相对接近于Oki对萎缩分裂的定义39.然而,计算出氧转化所需的能量(R1= R2= Me≈7 kJ mol−1)40.我们推断,三芳氧鎓支架中的芳香环与不同长度和柔韧性的连接物的连接应该增加氧转化的屏障,同时也保持了其他三芳氧鎓离子所表现出的稳定性(图2)。1 c)。足够高的对映异构势垒(我们定义为大于107 kJ mol)−1,t1/2rac = 25℃下7天;t1/2rac =手性样品的对映体纯度从100%降低到50%对映体过量的时间)将在实验室时间尺度上有效地锁定立体氧孤对的构型并产生螺旋手性分子41,42.我们推断,用重氮盐对二苯并呋喃支架进行分子内o -芳基化可以为这种分子提供一条可行的途径。
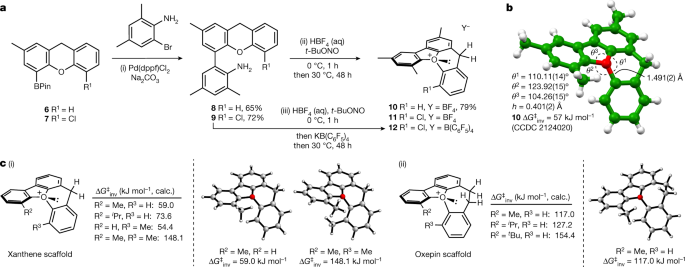
我们最初选择了二苯并呋喃-杂蒽支架作为我们的研究2杂蒽主链上的质子可以作为报告基团,在变温条件下测量反转势垒1H核磁共振波谱。我们制备了功能化的杂蒽6和7从商业资料(见第3页的补充信息详情);它们与4,6-二甲基-2-溴苯胺交叉偶联得到双芳基8和9.重氮化和分子内o -芳基化与氮的损失导致了五环四氟硼酸氧铵的形成10和11(无花果。2)。化合物的结构10单晶x射线衍射证实了这一点,表明该化合物在氧(氧周围的角和)处呈金字塔形θ1+θ2+θ3= 338.3(3)°,而二苯并呋喃的母体氧鎓为345(1)°43,以及顶点高度h= 0.401(2) Å,图2), C-O键最长长度为1.491(2)Å。二苯并呋喃环是平面的(内部C-O-C角为104.26(15)°),杂蒽的中心环呈船状构象,将相邻的两个芳环置于不同的平面上(图2)。2 b)。杂环杂蒽的C-O-C内角为110.11(14)°(母体杂环杂蒽本身为119.3°),表明在与苯并呋喃环融合时存在一定的角应变,尽管这似乎不会影响化合物的稳定性,该化合物可以在室温下无限期储存,而无需特别注意。低温1氢核磁共振谱测定其对映异构化势垒为58.3 kJ mol−1(见……第23页补充信息以进一步了解详情),这大大低于107千焦摩尔的估计值−1使构型稳定的分子得以分离。相反,氧鎓离子11仅作为一种暂态物种被观察到,我们最初认为这可能是四氟硼酸盐反离子作为亲核氟化物源(Balz - Schiemann反应)的结果。阴离子交换法得到的四氟硼酸重氮盐9变成不那么亲核的B(C6F5)4−提供反离子和环闭合12,但这种化合物在环境温度下72小时内会在溶液中缓慢分解。我们认为在二苯并呋喃-杂蒽支架上引入第二个取代基可能增加了菌株11和12中观察到的相对稳定性10.
一个(1) Pd(dppf)Cl2·CH2Cl2(5mol %), Na2有限公司3.(4个当量),PhMe/H2O (1:1, v/v), 95℃,24h;(2)住宅4(48% aq, 5个当量);t-BuONO(5等价物),CH2Cl2/IPA(1:1), 0℃,1 h, 30℃,48 h;(3)住宅4(48% aq, 5个当量);t-BuONO(5等价物),CH2Cl2/IPA(1:1), 0℃,1 h, KB(C6F5)4,然后30℃,48 h。b熔融五环氧鎓盐的晶体和分子结构10从单晶x射线衍射研究中得到。为清楚起见,省略了四氟硼酸盐溶液。括号内的数字表示标准不确定度。c, b3lypp - d3 (BJ)/6.31+G(d,p)基于二苯并呋喃-杂蒽核(i)和二苯并呋喃-苯并西平核(ii)计算了一系列氧鎓离子的转化势垒。h,概念化的斜三角形金字塔的高度,顶端为氧,相邻的o -芳基环上的碳组成底部;Calc,计算。
使我们能够合理地计算10以及更多取代化合物的反应性,比如11我们应用了b3lypp - d3 (BJ)/6-31+G(d,p)量子化学计算(见补充信息)。我们最初计算了氧鎓离子在苯并呋喃-杂蒽支架周围的转化障碍(图2)。2 c(我))。这与模型2-甲基氧鎓离子(R)的总体几何形状和金字塔反转势垒的实验值非常吻合2= Me, R3= H: 59.0 kJ mol时计算−1);其他层次的理论和基集给出了类似的定量结果。这些计算还表明,增加取代基R的大小2会导致反转势垒增加(73.6 kJ mol−1R2=我公关,R3= H),氧的锥体化有轻微的增加。将(甲基)取代转移到杂蒽部分,预测的对映异构化势垒与先前计算的(R)相似2= h, r3= me54.4 kJ mol−1),但低于理想的结构稳定性水平。为了研究取代基的加入对两个环的影响,我们研究了双烷基取代氧鎓(R2= R3=我)。这导致预测的对映异构化势垒增加到148.1 kJ mol−1但也导致了一些几何上的变化,这可能解释了观察到的分子的不稳定性,比如11和12在环境温度下。计算出氧鎓氧周围的角和为345.1°(R)2= R3= Me),与母体二苯并呋喃氧鎓离子相似,但我们观察到外部C-O-C角显著增加至129°,顶点高度降低(h= 0.33 Å),与氧周围锥体化的减少相一致。我们还观察到最长的C-O键进一步延长至1.51 Å。这是烷基取代基之间的空间排斥力的结果,这导致了杂蒽环的扭曲和填充在其中的船状构象的变形10.计算了一系列高同速键分离反应焓44使我们能够估计从一个化合物,如10(右1= H)到含有额外烷基(R)的1= Me)为16.7 kJ mol−1(见……第34页补充信息详情)。为11计算出的焓差10(45.6 kJ mol−1),可能表明电子和空间的贡献。我们可以得出结论,发展具有足够大的反转势垒的氧鎓离子,通过在该环体系上添加多个取代基而不影响稳定性来获得构型稳定性可能是一个挑战。
构型稳定分子的设计要求我们最大化基态和过渡态之间的差异。对于六元环,我们试图通过安装更大的R来破坏TS的稳定3.取代基)也不可避免地导致GS失稳。二氢二苯并西平具有非平面结构,我们设想额外的sp3.七元环中的碳(相对于杂蒽)可以避免GS中的空间不稳定。相反,我们推断当分子在TS中向平面运动时,额外的sp3.碳会积极地导致TS不稳定和更高的转化势垒。
我们计算了含氧素的氧离子的GS和TS结构(图2)。2 c (2))。从六元环变为七元环时,反转势垒从59.0 kJ mol增加到117.0 kJ mol−1(R2= Me, R3= H),增广到127.2 kJ mol−1154.4 kJ mol−1在引入较大的iso丙基,叔分别是-丁基。在计算得到的二氢二苯并西平GS结构中,氧的角和一般低于杂蒽系,并随着取代基尺寸的增大而减小;这与七环系列中更高的顶点高度和更高的氧金字塔化是一致的。
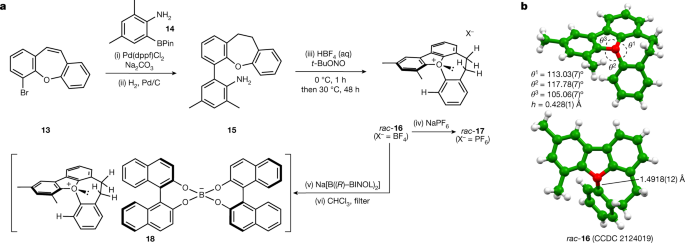
有了这些信息,我们专注于合成含七环的化合物,通过使用与之前采用的策略相似的方法:二苯并西平13(四步制得)与芳基硼酯交叉偶联14以67%的产率生产含二芳基的中间体。加氢给15在标准条件下将其重氮化,并轻轻加热至30°C,以实现o -芳基化并产生四氟硼酸氧铵rac-1675%产率(图2)3)。六氟磷酸钠反离子复合反应合成氧鎓离子rac-17收率为56%。钖tetrafluoroboraterac-16和方法rac-17是室温稳定的固体,可以无限期储存,不需要特别的预防措施。的结构rac-16被单晶x射线衍射研究证实(空间群P−1),这说明了氧环的预期褶皱构象和氧周围原子的锥体排列(氧周围的角度总和为335.9°,图5)。3 b)。顶点高度h= 0.428(1) Å,反映了氧相对于10.外C-O-C角为117.78(7)°,内oxepin C-O-C角为113.03(7)°;这些构成了相对较小的角度偏差,与在母体杂环中观察到的角度偏差相一致,并且与没有经历重大角度应变的环系统相一致。计算出的高同速反应焓表明氧鎓离子16比1013.4 kJ mol−1.对晶胞的检查没有显示任何短的C-H或C-C距离小于正常的范德华接触距离,这表明氧离子的构象不受晶体填充的影响。最长的C-O键长为1.4918(12)Å;这比苯并呋喃衍生的三苯基氧鎓离子(1.459(6)Å)和四苯基硼酸三苯基氧鎓的平均C-O键长度(1.47 Å)要长。
一个(1) Pd(dppf)Cl2·CH2Cl2(5mol %), Na2有限公司3.(4个当量),PhMe/H2O (1:1, v/v), 95℃,24 h(产率67%);(2) H2(g, 1个大气压),Pd/C (2.5 mol%), EtOAc, RT, 16 h(定量);(3)住宅4(48% aq, 5个当量),t-BuONO(5等价物),CH2Cl2/异丙醇(1:1),0°C, 1 h然后30°C, 48 h(75%的收益率);(iv) NaPF6(aq), CH2Cl2(56%的收益率);(v) Na [B ((R)−BINOL)2](1.0等效),MeCN, RT,然后CH2Cl2,用清水冲洗;(vi)溶于CHCl3.调节浓度。b.熔融五环氧鎓盐的晶体和分子结构rac-16从单晶x射线衍射研究中得到。为清楚起见,省略了四氟硼酸盐溶液。括号内的数字表示标准不确定度。h,概念化的三角形斜金字塔的高度,顶端是氧,相邻的o -芳基环上的碳形成底部。
治疗rac -16用化学计量量的钠-(R)-二酚硼酸盐完全转化为1:1的非对映异构体盐混合物(18,无花果。3.和19(图中未显示))。利用这两种盐在氯仿中的不同溶解度,可以沉淀一种盐,得到富集的非对映异构体对18(比94:6-99:1)。我们无法培养出适合于x射线分析非对映异构体富集盐的晶体18因此,我们试图通过用过量的四氟硼酸搅拌,在高度非对映异构体富集的样品中交换反离子。从这种混合物中,我们能够分离出所需的四氟硼酸盐晶体16;这在P212121的绝对构型P-(R)O(由Flack参数的细化决定)x对比三个独立晶体的x射线衍射数据集;CCDC 21911038 - 2191040)45的绝对构型,这也表明了氧鎓离子的绝对构型18(见第19页)补充信息)。探讨了二氯甲烷溶液的构型稳定性18在25°C下,观察到7天内非对映异构体比例有微小变化。根据这些数据和55:49 .5 (18,P-(R)O, (R);19,米-(年代)O,(R)),我们可以计算出螺旋反转的势垒为111.8±0.1 kJ mol−1(对于P-(R)O, (R)18来米-(年代)O, (R)19111.7±0.1 kJ mol−1(对于米-(年代)O, (R)19来P-(R)O, (R)18转换);在较高温度(超过50°C)下检验平衡的尝试导致分解速度快于平衡。我们还能分解六氟磷酸氧铵rac-17用手性固定相高效液相色谱法测定其对映异构势垒为111.0±0.1 kJ mol−1.这表明反离子对反转势垒大小的影响可能可以忽略不计,这与非对映异构体盐的观测值一致18和19(它们几乎是能量简并的)
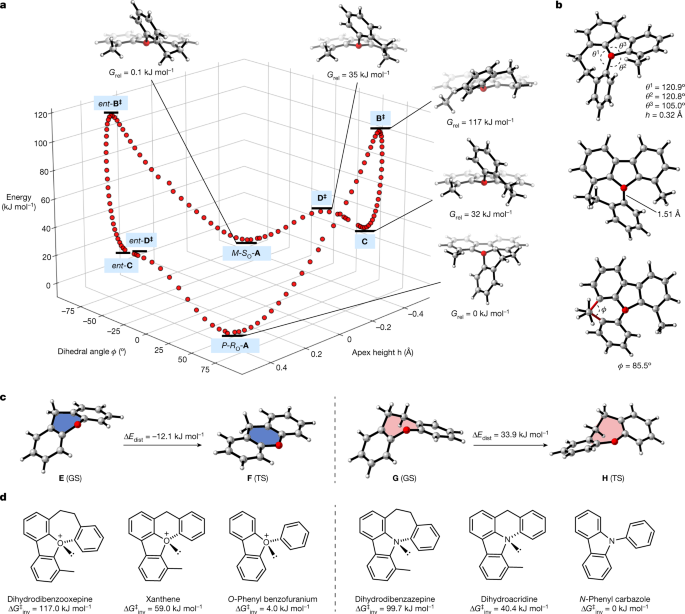
在实验中确定的反转势垒17和18(111.0-111.8 kJ mol−1)接近计算预测值(117.0 kJ mol)−1)。该氧鎓离子可逆对映异构化的计算反应能分布如图所示。4(ref。46);这表明对映异构化过程来自P-(R)O一个由一个高势垒螺旋反转和一个低势垒构象弛豫与七元环有关。过渡结构(TS)B对于螺旋反转(Grel= 117kj mol−1)在氧上具有倒金字塔的几何形状,尽管从GS中减少了一个(h= 0.32 Å,氧周围的角度和为346.7°B相对于335.9°一个)。氧为三角形平面的结构位于反应坐标的前面一个来B;这也证明了o型反转与分子螺旋手性的整体反转直接相关。在TSB,内部的oxepin和外部的C-O-C角都接近121°(图2)。4 b),这代表了氧原子周围的结构与GS的显著变化。与GS相比,oxepin环上的C-O键的长度也被观察到(1.51对1.49 Å)。TSB直接通向中间体C(Grel= 32 kJ mol−1),其中oxpin环呈船状构象;这经历了一个简单的环翻转通过TSD(Grel= 35 kJ mol−1)到GS结构中更稳定的船状构象米-(年代)O一个.解释含氧平的氧鎓离子的反转势垒大于40kj mol的原因−1比含杂蒽的类似物高,我们计算了氧鎓离子中六元和七元环的环应变在从GS到TS的过程中是如何变化的(图2)。4摄氏度)。在含杂蒽的体系中,船状的GSE变成几乎完美的平面TSF通过两个芳香环在同一平面内的运动。这导致了六元杂环12.1 kJ mol的应变降低−1.这是由于杂环的角应变有所缓解,这可以从内部C-O-C角从111.0°增加到116.6°(GS到TS)中看出。在这个体系中,TS类似于蒽本身的GS构象。相比之下,应变增加了33.9 kJ mol−1二氢二苯并西平环中G对TSH.达到TS几何演示在H,两个芳香环扭曲,使七元环反转。这通过扭转应变的组合(在两个sp之间)提高了能量3.(H-C-C-H扭度= 38.1°)),主链之间烯丙基应变增加3.碳氢键与芳环的内角应变和两个芳环的平面度有轻微偏差。氧鎓离子中的七元环构象G是船状的,类似于二氢二苯并西平本身:在TSH大大提高能量。氧孤对的离域沿反应坐标变化,这也是区分二氢二苯并西平和杂蒽衍生氧鎓离子的一个重要来源。自然键轨道47计算结果表明,氧的孤对离域到相邻π体系中可以稳定倒转TS。对于杂蒽氧鎓离子,氧的平面度增加可以使倒转TS稳定54.1 kJ mol−1相对于GS,而对于二氢二苯并西平氧鎓离子,它更低,为12.0 kJ mol−1,差值为33.1 kJ mol−1.七元环氧鎓主链中应变的增加抑制了反转TS中的平面化,减小了孤对离域的程度,从而增加了活化能势垒。
为了研究杂原子的身份如何影响反转势垒,我们计算研究了这类氧鎓离子及其氮类似物(图2)。4 d)。计算得到的三芳氧鎓离子的转化势垒系统地高于它们的三芳胺对应物。这可以根据杂原子的再杂化阻力来解释,氧离子的再杂化阻力更大(见《原子动力学》第38页)补充信息)。对于氮类似物,在反转TS结构中存在较大的孤对离域。这与二氢二苯并西平氧鎓(Δ)的计算结果一致G‡发票= 117.0 kJ mol−1)和二氢二苯卓(Δ)G‡发票= 99.7 kJ mol−1)体系,表明势垒高度既取决于环结构提供的几何约束,也取决于杂原子的同一性。
参考文献
《氮转化:实验与理论》。Fortschr。化学。Forsch。15, 311-377(1970)。
Baechler, R. D.和Mislow, K.结构对非环膦锥体转化速率的影响。j。化学。Soc。92, 3090-3093(1970)。
Andersen, k.k., Cinquini, M. & Papanikolaou, N. E.三芳基磺酸盐的合成和立体化学。j . Org。化学。35, 706-710(1970)。
罗克,A,艾伦,L. C.和米斯洛,K.金字塔反演。Angew。化学。Int。艾德,心血管病。9, 400-414(1970)。
陈洪生,阮秋宁,陈洪生,陈志强,陈志强,陈志强,陈志强,陈志强,陈志强,陈志强,陈志强,陈志强。j。化学。Soc。141中文信息学报,15951-15962(2019)。
Meerwein, H., Hinz, G., Hofmann, P., Kroning, E. & Pfeil, E. Über tertiäre oxoniumsalze I.。j . Prakt。化学。147, 257-285(1937)。
兰伯特,J. B. & Johnson, D. H.三价氧的立体化学和转化。j。化学。Soc。90, 1349-1350(1968)。
Tröger, J. Ueber eingemittelst . nascirenden甲醛研究进展。j . Prakt。化学。36, 225-245(1887)。
Prelog, V. & Wieland, P. Über die spaltung der Tröger 'schen base in opsche对映体,in beitrag zur stereochemistry des drewertigen stickoff。Helv。詹。学报27, 1127-1134(1944)。
Rigol, S., Beyer, L., Hennig, L., Sieler, J.和Giannis, a . Hunlich碱基:一个世纪后的发现、合成和结构解析。Org。列托人。15, 1418-1420(2013)。
Boratyński P.J, Zielińska-Błajet M. & Skarżewski J.金鸡纳生物碱衍生物及其应用。生物碱化学。医学杂志。82, 29−145(2019)。
黄,S.等。含多立体元素的手性氮平骨架的有机催化对映选择性构建。Angew。化学。Int。艾德,心血管病。60[j] .中文信息学报,2011(5):555 - 556。
Rowley, J. H., Yau, S. C., Kariuki, B. M., Kennedy, A. R.和Tomkinson, N. C.。Org。Biomol。化学。11, 2198-2205(2013)。
Walsh, m.p., Phelps, j.m., Lennon, m.e., Yufit, d.s.和Kitching, m.o.铵离子的对映选择性合成。自然597, 70-76(2021)。
柯普尔,g.w, Sagatys, d.s, Krishnamurthy, g.s.和Miller, s.i.3.)和相关的平面(=XY)物种。j。化学。Soc。89, 3396-34051(1967)。
Penner, g.h, Polson, k.m, Daleman, S. & Reid, K.两类铵盐分子动力学和几何结构的氘核磁共振研究3.)+X−和C6H5米(CH3.)3.+我−.可以。j .化学。71, 417-426(1993)。
Mikata, Y., Fujimoto, T., Noko, I.和Kondo, S.铜(II)配合物与二聚胺衍生配体的氧原子手性的差异。欧元。j . Inorg。化学。2012, 4310-4317(2012)。
Mikata, Y., Sugai, Y., Obata, M., Harada, M. & Yano, S.在一系列糖悬垂二聚胺铜(II)配合物中,醚氧原子与金属中心的不对称配位诱导的新型氧手性。Inorg。化学。45, 1543-1551(2006)。
关于通过亲电溴化生物合成海洋天然产物邻苯二烯家族的假设。Org。列托人。8, 6055-6058(2006)。
Murai, A. in天然产物综合化学第一版(eds Barton, d.h.r., Meth-Cohn & O. Nakanishi, K.) 303−324 (Elsevier, 1999)。
Kikuchi, H., Suzuki, T., Kurosawa, E. & Suzuki, M.15从红藻中提取的具有新型碳骨架的非萜类化合物Laurenda培山田。公牛。化学。Soc。日本。64, 1763-1775(1991)。
一个统一的立体化学分析形成的卤化C15-醋酸原素中环醚laurencia通过分子内溴离子辅助环氧化物开环并与模型环氧化物进行实验验证。j . Org。化学。77科学通报,9574-9584(2012)。
金,B.等。通过有机硒介导的分子内羟基醚化合成(−)-月桂素的仿生不对称全合成。j。化学。Soc。130, 16807-16811(2008)。
张,Yaw, N. & Snyder, S. A.一般合成方法laurencia由潜在的仿生环扩张授权的天然产品家族。j。化学。Soc。141中文信息学报,7776-7788(2019)。
Stoyanov, e.s.等。R3.O+H···+氢键:指向四配位的氧二碘(2+)离子。j。化学。Soc。134, 707-714(2012)。
Meerwein, H., Bettenberg, E., Gold, H., Pfeil, E. & Willfang, G. Über tertiäre oxoniumsalze II。j . Prakt。化学。154, 83-156(1940)。
克拉格斯,F.和荣格,H. A.合成和特征schaften - eines双环氧鎓盐。化学。的误码率。98, 3757-3762(1965)。
周建军,周建军。环氧鎓离子及其相关结构。国家科学院学报美国。62, 52-55(1969)。
Olah, G. A., Doggweiler, H., Felberg, J. D.和Frohlich, S. Onium ions。33.(三甲基硅基)-和[(三甲基硅基)甲基]氧鎓和-卤鎓离子。j . Org。化学。50, 4847-4851(1985)。
Etzhorn, m.s et al. 1 - Oxoniaadamantane。欧元。j . Org。化学。2008中文信息学报(英文版),2008。
Mascal, M, Hafezi, N., Meher, N. K. & Fettinger, J. C. oxtriquinane和oxtriquinacene:特殊氧鎓离子。j。化学。Soc。130中文信息学报,2008)。
Mascal, M., Hafezi, N.和Toney, M. D. 1,4,7-三甲氧基三奎烷:SN2在叔碳上的反应。j。化学。Soc。132, 10662-10664(2010)。
Gunbas, G.等。极端的恶三醌和创纪录的C-O键长。Nat,化学。4, 1018-1023(2012)。
Suzuki, H. & Muratake, H.功能化的恶三醌及其在质子溶剂中的结构平衡。化学。制药。公牛。62, 921-926(2014)。
Nesmeyanov, A. N., Makarova, L. G.和Tolstaya, T. P.异分解的化合物(二苯基卤素和三苯基氧鎓盐)。四面体1, 145-157(1957)。
沃特金斯,M. I,叶,W. M,奥拉,G. A.和鲍,R.。23.氧鎓离子的结构:六氟磷酸三乙基氧鎓和四苯基硼酸三苯氧鎓的x射线晶体学研究。j。化学。Soc。104, 2365-2372(1982)。
托尔斯泰,t.p.等。亲核取代O-苯二苯铀和10-苯黄嘌呤离子。拉斯。化学。公牛。46, 789-797(1997)。
helwinkel, D. & Seifert, H. Ringschlußreaktionen von 2 ' -杂取代间联苯-2-重氮-salzen zu (spiro)环化四芳基铵-salzen和三苯[b.d.f]azepinen。化学。的误码率。105, 880-906(1972)。
好的,我是m立体化学主题第14卷(编Allinger, n.l., Eliel, e.l.和Wilen, s.h.) 1-81 (Wiley, 1983)。
Lu, M.等。氮和氧的苝酰x-铵离子。Org。化学。前面。6, 2640-2646(2019)。
Bosson, J, Gouin, J. & Lacour, J.阳离子三角烯和螺旋烯:这些不寻常染料的合成、化学稳定性、光学性质和扩展应用。化学。Soc。牧师。43, 2824-2840(2014)。
吴,Y.-T。,H一个yama, T., Baldridge, K. K., Linden, A. & Siegel, J. S. Synthesis of fluoranthenes and indenocorannulenes: elucidation of chiral stereoisomers on the basis of static molecular bowls.j。化学。Soc。128, 6870-6884(2006)。
Zhukhlistova, n.e., Tishchenko, g.n., Tsarev, d.a.和Tolstaya, t.p.晶体和分子结构O-phenyldibenzofuranium tetrafluoroborate。Kristallografiya42, 863-869(1997)。
惠勒,S. E, Houk, K. N., Schleyer, P. V. R. & Allan, W. D.。j。化学。Soc。131, 2547-2560(2009)。
Flack, H. D.关于对映纯极性估计。Acta Crystallogr。A39, 876-881(1983)。
Reist, M., Testa, B., Carrupt, P. A., Jung, M. & Schurig, V.外消旋化,对映异构化,非对映异构化和外映异构化:它们的意义和药理意义。手性7, 396-400(1995年)。
格兰德宁,e.d.等。NBO v. 7.0。威斯康星大学麦迪逊分校理论化学研究所https://nbo6.chem.wisc.edu/biblio_css.htm(2018)。
致谢
EPSRC通过生物学和医学合成博士培训中心(EP/ L015838/1)为学生(O.S.和M.V.P.)提供财政支持,并通过DTP奖学金(EP/T517811/1;项目没有。2446204)。R.P.感谢美国国家科学基金会(CHE-1955876)的支持,以及由美国国家科学基金会(ACI-1532235和ACI-1532236)、科罗拉多大学博尔德分校和科罗拉多州立大学以及极端科学与工程发现环境(XSEDE)支持的RMACC峰会超级计算机的计算资源,通过分配gt - che180056。我们感谢A. Thompson(牛津大学)在x射线晶体学和P. Solon在高效液相色谱测量方面的协助。根据EPSRC的开放获取条件,对本次提交的作者接受的手稿适用CC-BY许可。
作者信息
作者及隶属关系
贡献
o.s., M.V.P, m.j.h., r.p., J.W.B.和M.D.S.构思并设计了这项研究。O.S.和M.J.H.进行了合成实验并分析了所有化合物的数据。os进行了x射线晶体学。M.V.P.和R.P.进行了计算研究。存在的非政府组织)却是事实。,M.V.P M.J.H, R.P J.W.B.和M.D.S. cowrote。有关计算的信件应寄给R.P.;所有其他信件应寄给M.D.S.和J.W.B.
相应的作者
道德声明
相互竞争的利益
作者声明没有利益竞争。
同行评审
同行评审信息
自然感谢Jonathan Clayden, Ganna Gryn'ova和其他匿名审稿人对这项工作的同行评审做出的贡献。
额外的信息
出版商的注意施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,该协议允许以任何媒介或格式使用、共享、改编、分发和复制,只要您适当地注明原作者和来源,提供知识共享许可协议的链接,并注明是否进行了更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查阅本许可证副本,请浏览http://creativecommons.org/licenses/by/4.0/.
关于本文
引用本文
史密斯,O.,波佩斯库,m.v.,辛德森,M.J.et al。螺旋手性氧鎓离子中立体氧的控制。自然615, 430-435(2023)。https://doi.org/10.1038/s41586-023-05719-z
收到了:
接受:
发表:
发行日期:
DOI:https://doi.org/10.1038/s41586-023-05719-z